2018信州総文祭
広島はレモン生産量国内NO.1! ビタミンCの「すっぱい!」のヒミツは私たちが解明する!
【化学】広島県立広島井口高校 科学部

■部員数 18人(うち1年生12人・2年生4人・3年生2人)
■答えてくれた人 晴木啓二朗くん(2年)
ビタミンCの変化についての研究~ビタミンCはなぜ酸っぱいのか~
体の維持に不可欠なビタミンCの性質に着目!
広島県はレモンの生産量が日本で一番多いことで知られており、2014年度の全国のレモンの生産量の60%が広島県産のものでした。そこで私たちはレモンについてよく調べてみようと考え、レモンの中に多く含まれているビタミンCを研究のテーマとしました。
ビタミンCは、L-アスコルビン酸とも呼ばれます。抗壊血病因子であり、体内では抗酸化物質としてはたらくビタミンです。これはヒトが体を維持するうえで必要な物質ですが、ヒトはビタミンCを体内で合成することができないため、食品から摂取する必要があります。
しかし、ビタミンCは熱に弱く、酸化されやすいという特徴があるため、調理法によっては調理の過程で大きく変化してしまうことが考えられます。そこで私たちは、ビタミンCの壊れにくい調理法を探すため、どのような条件でビタミンCが壊れてしまうのか調べることにしました。
調理の過程でビタミンCの変化はどのように起こるか?
ビタミンC(L-アスコルビン酸)は酸性で存在しており、中性では一価の陰イオンとして、塩基性では二価の陰イオンとして存在することが知られています。また、エンジオール構造を持っているため、酸化するとデヒドロアスコルビン酸に変化しますが、この変化は可逆的です。また、デヒドロアスコルビン酸が加水分解して、2,3-ジケトグロン酸へ変化しますが、この変化は不可逆的です。

私たちは今回の研究をするにあたり、「加熱」「液性の変化」「紫外線(UV)」「金属イオン」という4つの要因によってL-アスコルビン酸の変化が促進されるのではないかと考えました。さらに、これらの要因を組み合わせることで、単一の条件を変化させたときよりも、L-アスコルビン酸はより一層変化しやすくなるのではないかという仮説を立て、実験を開始しました。
濃度決定の実験〜加熱と液性の条件
最初に、L-アスコルビン酸の濃度決定を行います。チオ硫酸ナトリウム水溶液を用いて正確な濃度を測定したヨウ素ヨウ化カリウム水溶液で、L-アスコルビン酸を滴定して濃度を決定しました。いずれの実験もこの手順で得られた0.010 mol/LのL-アスコルビン酸溶液を用い、0.5時間ごとに1.5時間後まで濃度を測定しました。
まず加熱による濃度変化を調べました。加熱前から加熱後では濃度が7.6 %減少していたことが確認できました。次に加熱操作に加え、液性の条件も変更して実験を行いました。水酸化ナトリウム水溶液を加えて中和し、pH 2、pH 7、pH 11に調整しました。

次にTLC(薄層クロマトグラフィー)で展開したところ、中性の条件で加熱した場合は、L-アスコルビン酸の濃度の減少率は56.6 %となり、酸性条件下に比べ明らかに減少率が大きいことがわかります。
L-アスコルビン酸と、その酸化物であるデヒドロアスコルビン酸は、異なる位置にスポットを示します。
また、中和していない溶液と中和後の溶液の場合も異なる場所にスポットを示します。一方、中和したものと中和後加熱処理をしたものでは、同じ場所にスポットを示しました。
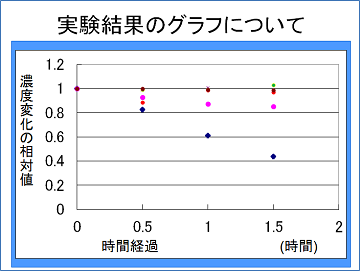
濃度変化を観察した結果をグラフにすると、pH 2、pH 7のときにはほとんど変化は見られませんでしたが、pH 11のときは1.5 時間後に濃度が非常に小さくなっていることが確認できます。
金属イオンやUV照射による濃度変化はあるのか?
次に、pHを変化させUVを照射したところ、pH 2では変化が見られなかった一方、pH 11では濃度が大きく減少しました。

今度は、Cr3+, Mn2+, Co2+, Ni2+, Cu2+, Zn2+, Al3+, Fe3+の8種類の金属イオンを、ビタミンCと同物質量加えて実験を行いました。
その結果、濃度変化の傾向はCu2+ 、Fe3+ と、そのほかの金属イオンの3つに分けることができました。
まず、Cu2+ 、Fe3+ 以外の金属イオンについては、添加しても濃度変化は見られませんでした。UV照射をした場合も、同様に変化はありませんでした。

しかし、液性をpH7にしたところ、時間が経過するにつれ濃度が減少することが確認できました。特にMn2+が最も変化が大きく、Ni2+はあまり変化しませんでした。

TLCで展開した様子を見ると、金属イオンを添加したものとそうでないものでは、異なる位置にスポットを示しています。
しかし、金属イオンを加えても、デヒドロアスコルビン酸を生成していないこともわかります。また、どの金属イオンを加えた場合も極性の低い位置にスポットが現れました。

次に、pH 7の溶液にUV照射した結果です。UV照射しなかった場合よりも変化の度合いが大きくなっていますが、各金属イオンの変化の様子を比べると、UVを照射しなかった場合と同様の順になっています。
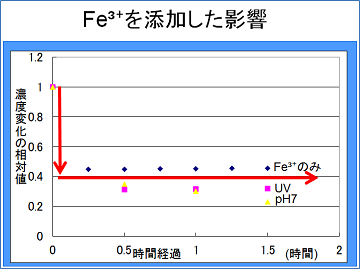
一方Fe3+を添加した場合です。この場合は、L-アスコルビン酸の濃度がすぐに半分以下に減少し、その後は時間が経っても一定でした。さらに、UVを照射したり中性条件下にしたりすると、時間が経つにつれ濃度はやや減少することがわかりました。
このことから、三価の鉄イオンが還元されたのではないかと考えられます。

また、Fe3+の添加量を2倍にして、ビタミンCの2倍量を加えたところ、Fe3+添加後すぐにL-アスコルビン酸の濃度は0付近になりました。
これらの結果から、Fe3+がL-アスコルビン酸に対して反応する仕組みは、他の金属イオンとは全く異なるのではないかと考えました。
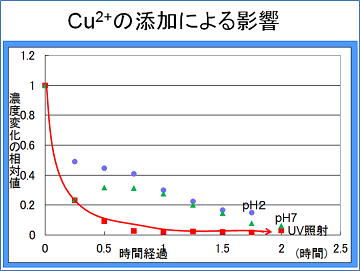
最後に、Cu2+を添加した場合は、どの条件下でも濃度変化が見られたものの、pH 2とpH 7では、その様子に大きな違いはありませんでした。しかし、UVを照射したときに、最も大きな濃度変化が見られました。
ビタミンCの「すっぱさ」が加熱によって減少する原因
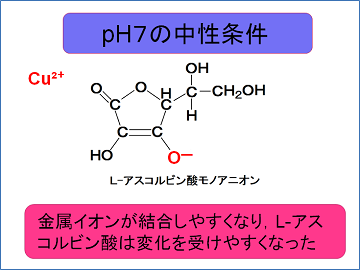
これらの実験結果を踏まえると、L-アスコルビン酸の変化について以下のようなことが考えられます。
まず、pH 2の酸性条件下では加熱、UV照射、金属イオンの添加いずれに対しても変化は小さく、安定しています。ところが、pH 7の中性条件下では金属イオンによる変化が大きくなり、酸性条件下よりも不安定になります。
この原因として、中性条件下ではL-アスコルビン酸は一価の陰イオンとして存在しているため、金属イオンと結合しやすくなり、変化を受けやすくなったということが考えられます。
さらに、pH 11の塩基性条件下ではUV照射による影響が大きくなりました。これは、塩基性条件下で二価の陰イオンとして存在している場合、UV照射により活性化され、変化しやすくなるためではないかと考えました。
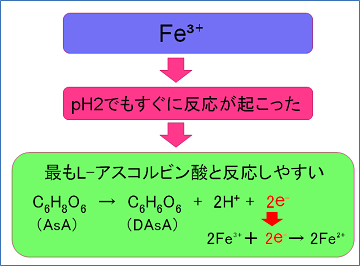
また、Fe3+を添加した際は、安定しているはずのpH 2でもすぐに変化が起こりました。
これは、L-アスコルビン酸とFe 3+が1:2の物質量比で反応していたことからも、Fe 3+が酸化剤として働いたためではないかと推測できます。そのため、L-アスコルビン酸との反応の様子が他の金属イオンと異なるのではないかと考えました。
しかし、TLC展開をした様子を見ると、デヒドロアスコルビン酸の位置にスポットは見られず、デヒドロアスコルビン酸は生成していないことがわかります。
さらに、L-アスコルビン酸よりもやや極性の低い位置にスポットが現れたという点も、他の金属イオンと同様の傾向でした。Fe 3+を添加した際の特徴としては、極性の高い位置に濃いスポットが見られましたが、この原因はわかっていません。
Cu2+を添加した場合は、酸性条件下でもUV照射をした場合でも不安定化し、変化が大きくなりました。このことから、L-アスコルビン酸はCu2+との結合で活性化し、変化しやすくなると推測できます。また、他の金属イオンに比べ、UV照射による活性化の度合いが大きいのではないかと考えました。
さらに、Cu2+、Fe3+を添加したとき以外の場合では、加熱、UV照射、金属イオンの添加、すべての条件変化に対してpH 2で安定していたため、L-アスコルビン酸の還元力、すなわち抗酸化性を維持するためには、酸性条件下である必要があるため、L-アスコルビン酸は酸性であり、ビタミンCを多く含むレモンは酸っぱく感じるのだと私たちは考えました。
調理においては、酸性条件を維持することで加熱等の影響によるビタミンCの変化を防ぐことができるといえます。鉄イオンについては、pH 2であっても影響してしまうため、私たちは、鉄表面をガラスコーティングしているホーロー鍋を使用することを推奨します。
今後は、今回調べた条件以外でもL-アスコルビン酸の濃度変化を調べ、変化しやすい条件を調べていきたいと考えています。
■研究を始めた理由・経緯は?
部員の1人が食品に興味があったからです。
■今回の研究にかかった時間はどのくらい?
1日あたり2時間で、4カ月くらいかかりました。
■今回の研究で苦労したことは?
1回の測定に2時間かかり、その間3回測定をするので、その待ち時間が長かったことです。
■「ココは工夫した!」「ココを見てほしい」という点は?
研究のまとめに力を入れているので、研究についてとてもわかりやすくなっていると思います。
■今回の研究にあたって、参考にした本や先行研究
「ビタミンCの辞典」石上昭人(東京堂出版)
■今回の研究は今後も続けていきますか?
今後は、ビタミンCに他のビタミンを混ぜて、その変化を調べていきたいです。
■ふだんの活動では何をしていますか?
新しい研究テーマを設定して実験をしています。また、ウーパールーパー、メダカ、イモリなどの生物の世話などをしています。
■総文祭に参加して
他の発表はとてもレベルが高く、理解するのが難しかったです。また、次の研究に向けてとても参考になることが多かったです
 みらいぶっくグループ
みらいぶっくグループ


















